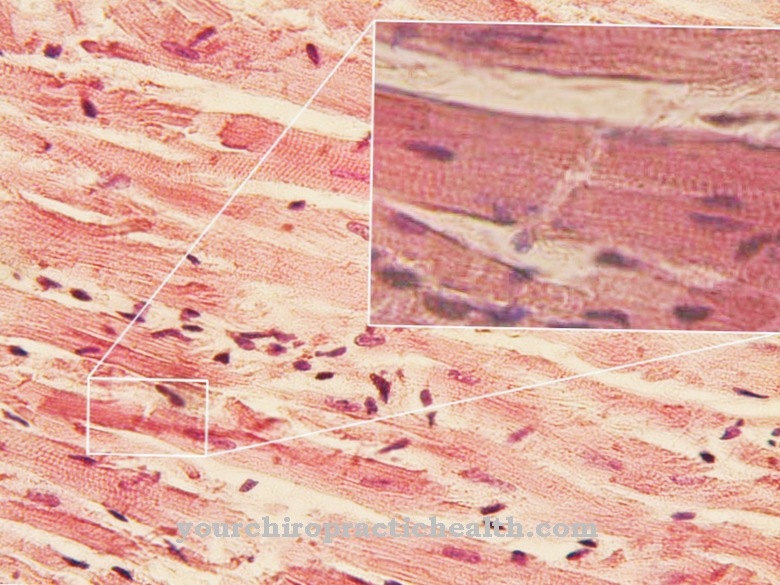
Скрининг анеуплоидии используется для определения числовых хромосомных аберраций в эмбрионах, созданных in vitro и предназначенных для имплантации. Это цитогенетическое исследование, при котором можно определить только числовые аберрации определенных хромосом. Таким образом, скрининг на анеуплоидию является формой предимплантационной диагностики (ПГД).
Что такое скрининг на анеуплоидию?

Термин «скрининг на анеуплоидию» используется для обобщения методов цитогенетического исследования, которые могут дать указание на числовые аберрации в определенных хромосомах при экстракорпоральном оплодотворении (ЭКО). В принципе, скрининг на анеуплоидию может предоставить показания для нуллосомии, моносомии и полисомии, такие как Б. дают трисомию.
При нуллосомии пара хромосом полностью отсутствует, при моносомии отсутствует одна гомологичная хромосома из пары хромосом, а при полисомии имеется более двух гомологичных хромосом для конкретной пары хромосом. Самая известная полисомия - трисомия 21, которая приводит к синдрому Дауна. Поскольку большинство числовых хромосомных аберраций, особенно моносомий, являются летальными, то есть приводят к естественным абортам, выкидышам или мертворождению, в матку имплантируются только эмбрионы без видимых хромосомных аберраций.
Это должно повысить вероятность успеха ЭКО, но некоторые хромосомные аберрации не обязательно фатальны, но приводят к аномалиям и серьезным ограничениям в дальнейшей жизни, например, при синдроме Дауна или Тернера. Вот почему в некоторых странах существует общий запрет или строгие ограничения на этот тип предимплантационной диагностики (ПГД) по этическим причинам.
Функция, эффект и цели
Скрининг на анеуплоидию используется только при экстракорпоральном оплодотворении. Самая важная цель - перенести в матку только эмбрионы без распознаваемых хромосомных аберраций, чтобы получить максимально возможные шансы на успех беременности с помощью искусственного оплодотворения. В принципе, можно провести различие между двумя методами диагностики полярных тел и исследованием предимплантационного эмбриона. Первый метод заключается в исследовании полярных тел еще не оплодотворенной яйцеклетки.
Здесь проверяется только возможная анеуплоидия яйцеклетки. Это делается исходя из предположения, что около 90% анеуплоидий имеют материнское происхождение. Это не ПГД в более узком смысле, а предпочтительный диагноз, потому что не произошло оплодотворения, то есть слияния яйцеклетки со сперматозоидами. С другой стороны, скрининг на анеуплоидию предимплантационного эмбриона на ранней стадии бластулы квалифицируется как ПГД, потому что обследование относится к «настоящей» эмбриональной стадии - даже если это очень ранняя стадия, всего несколько дней назад.
При диагностике полярных тел два полярных тельца, которые яйцеклетка формирует во время первого и второго мейоза, прежде чем она сливается со сперматозоидом, удаляются и исследуются на анеуплоидию. Так называемый FISH-тест (флуоресцентная гибридизация in situ) используется для определения любой анеуплоидии, которая может присутствовать. До сих пор тест FISH позволял исследовать только хромосомы 13, 16, 18, 21, 22 и половые хромосомы X и Y. Хромосомы двойной спиральной структуры, расщепленные после мейоза, соединяются с хромосомно-специфическими ДНК-зондами с соответствующей комплементарной последовательностью ДНК.
Зонды ДНК отмечены разными флуоресцентными цветами. Гомологичные хромосомы можно подсчитать под световым микроскопом в полуавтоматическом процессе, чтобы можно было идентифицировать числовые аберрации. По аналогии с диагностикой полярных тел, скрининг на анеуплоидию проводится на предимплантационных эмбрионах, которые все еще находятся на стадии раннего бластомера. Однако теперь мы имеем дело с диплоидными наборами хромосом, двойная спираль которых сначала должна быть разделена, чтобы инициировать соединение хромосом с комплементарными ДНК-зондами.
Целью скрининга анеуплоидии в обоих методах остается положительный отбор яйцеклетки, оплодотворенной in vitro, до ее переноса в матку, чтобы достичь максимально возможного успеха для желаемой беременности. Часто обсуждаемая этическая проблема возникает из-за отрицательного отбора, который автоматически связывается с положительным отбором и который некоторые крайние критики любят использовать аргументы, чтобы приблизить его к эвтаназии. Еще одна этическая проблема связана с использованием ЭКО для создания так называемого ребенка-спасателя. Положительный отбор эмбрионов, созданных in vitro, можно использовать для культивирования всемогущих иммуносовместимых стволовых клеток, которые могут спасти жизни братьев и сестер с определенными заболеваниями посредством имплантации.
Риски, побочные эффекты и опасности
Сам скрининг на анеуплоидию, а также извлечение ядер клеток, которые необходимо исследовать, происходят вне организма и, следовательно, не связаны с какими-либо прямыми рисками или опасностями для здоровья и, следовательно, не имеют побочных эффектов. Фактические риски и опасности заключаются в том, что польза от скрининга аноиплоидии на бластомерах, то есть на предимплантационных эмбрионах, для увеличения вероятности успеха в отношении желаемой беременности еще не достигнута.
Общие системные проблемы возникают из-за завышенных ожиданий относительно точности результатов скрининга. Это касается как положительного, так и отрицательного результата. Положительный результат, т.е. обнаружена хотя бы одна хромосомная аберрация, связан с определенной неопределенностью. Может случиться так, что положительный результат ошибочно исключает трансплантацию соответствующей яйцеклетки, хотя в действительности хромосомного дефекта нет. Этот тип ошибочного диагноза связан не столько с самой процедурой, сколько с тем фактом, что эмбрионы на стадии бластулы могут иметь несколько клеток с хромосомными аберрациями.
С другой стороны, потенциальные родители ребенка ЭКО не должны быть уверены, что если тест на анеуплоидию отрицательный, то на самом деле хромосомная аберрация отсутствует. Другая опасность возникает при удалении необходимого количества клеток из эмбриона. Бывает, что взятые при биопсии клетки погибают и их уже нельзя исследовать. Поскольку биопсию больше нельзя повторить на том же эмбрионе, она больше не доступна для трансплантации из-за отсутствия результата теста. Также обсуждается, в какой степени биопсия влияет на фертильность эмбриона, так что это влияет на общую успешность беременности.





.jpg)




.jpg)



.jpg)
.jpg)